
自从环保部在2020年颁布了《芬顿氧化法废水处理工程技术规范》(HJ 1095-2020)以后,就引起了广泛的讨论。
那为啥人们都对于这个规范有如此多的看法呢?
主要是这个规范中给出的很多参数,范围太大,让人有一种无从下手的感觉。
例如芬顿试剂配比总,双氧水和亚铁的质量比值范围,就高达10倍的差异(1:1~10:1)。
给出这么大的范围,基本就和没说一样。
这就要求你在实际项目中,最终还是得动手做实验,拿最终的实验数据来确定工艺参数。
除此之外,你再细看,整个技术规范中,明里暗里让你去做实验才能确定的参数,就有4处!
那位说了:
“芬顿不就是酸、铁、双氧水、碱的一个药剂组合吗,为啥就不能在一个小范围内确定下来最合适的参数,怎么就非得做个实验呢?”
你要认为这是规范编纂者们偷懒耍滑,那可真是冤枉人家了。
之所以芬顿的技术规范不像其他规范一样,有可以直接参考的设计参数,还是和芬顿工艺的原理有关系。
但凡是有认真了解过芬顿工艺的人,都会发现其去除污染物的原理十分复杂。
准确地说是芬顿系统涉及到的反应太多,针对不同污染物的反应机理又都稍有区别,这就导致其牵扯的副反应太多。
我在研究相关论文时,有次竟然看到了有将近20个的反应方程式。
而且我也相信,这还不是最多的!
由此可见,芬顿反应的复杂,绝非其他工艺可以比拟。
但你要想弄清楚芬顿工艺的设计,还真就不能不理会其基本原理。
关于芬顿工艺原理的理解,以下部分是我的一家之言,如有不对之处,还希望共同探讨。
正所谓擒贼先擒王,任它芬顿的反应再多,但是万变不离其宗,学会了抓主放次,那就能保证研究的大方向不跑偏。
先讲芬顿的两个主要反应式:
Fe²+ + H2O2 → Fe³+ + ·OH + OH - (1) Fe³ + + H2O2 → Fe²+ + HO2· + H+ (2)
其中反应式(1),能够生成具备强氧化性的羟基自由基。
且生成的越多,处理的效果就越好。
所以它其肯定是大家最希望看到的,多多益善。
并且在这个化学方程式中,可以看出,1mol的双氧水可以对应形成1mol的羟基自由基。
这就意味着,1mol的双氧水对应1mol氧化能力的氧,也即1mol的COD值。
而双氧水的摩尔质量为34g/mol,COD的摩尔质量就是一个氧的摩尔质量,16g/mol。
所以按照反应式1计算得到的mCOD:mH2O2=16/34=47%。
这与技术规范的COD与双氧水给的参数(1:1~1:2)中最低值50%较接近。
但在实践中,芬顿工艺却可能会需要投加更多的双氧水去氧化降解COD,那这是为什么呢?
因为方程式(2)!
要知道在芬顿反应中,好不容易生成的羟基自由基,并不是都去和污染物反应了。
有的还和三价铁反应,把三价铁还原成亚铁。
这就是需要更多双氧水的原因。
那这里面还有一个问题,就是为什么技术规范会给定一个最高为1:1的比值呢?
这个双氧水少了理论值的一半啊!
这个问题我们放到后面讲。
那既然反应(2)会浪费双氧水,我们可不可以找一种不需要双氧水,就能把三价铁还原成二价铁的方法呢?
有啊,例如光芬顿、电芬顿等工艺,都是奔着这个目的去的。
但这里我并不打算详说了,因为光芬顿的原理更复杂,机理也难做,它不只要捕捉羟基自由基,还要捕捉空穴对。
但可以肯定的一点是,不论光芬顿还是电芬顿,其目的都是为了促进三价铁得电子生成二价铁。
这样就能解决一部分羟基自由基的浪费问题,提高了双氧水的利用效率。
当然随着技术发展,光电的作用早已不仅仅是促进亚铁的生成了。
国外的一些机构就尝试着做了一些将三价铁泥依靠生物还原成亚铁回用的研究。
但截止目前,此类研究的局限性依然很大,基本还没有走出实验室进行工业化的可能。
所以芬顿反应铁是在三价和二价来回转换的,这就产生了另外的几个问题。
问题1:亚铁离子既然是催化剂,那么其用量理应就会很少,为啥实际运行中却要投加这么多的亚铁呢?
问题2:亚铁离子特别是铁离子,容易遇碱沉淀,而一旦沉淀后,就极易失去催化活性,所以最佳pH这个条件又该怎么控制?
问题3:铁离子其实还特别容易与其他物质发生化学沉淀反应,例如硫离子、磷酸根等等,这个影响又该怎么破解?
针对以上问题,我尝试着解答如下,如果您有不同看法,也欢迎一起交流。
首先,针对问题1的解释,主要是反应(1)的速度要远远大于反应(2),这样就会导致铁离子的积累。
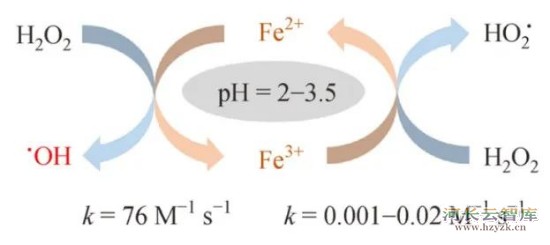
▲反应1与2的速度对比,数据出处《Dual-reaction-center catalytic process continuesFenton’s story》
而我们又知道,铁离子特别容易遇碱沉淀,一旦形成氢氧化铁,再想通过化学方程式(2)还原到二价铁,那基本就是不可能了。
所以就得需要不断补充二价铁。
但亚铁太高的话,对于芬顿反应的整体也不友好。
因为它的还原性太强了,好不容易产生的羟基自由基就特别容易将其氧化,白白浪费了宝贵的羟自由基资源。
所以在实际中,芬顿最好是将一定量的亚铁,缓慢或匀速的投加到反应池中,氧化的效果会好一些。
再来解释下问题2。
为了解决这个问题,人们通常都会把芬顿反应的水体环境调为酸性,控制pH在3~3.5左右(技术规范给的是3~4)。
但芬顿反应最佳的pH值范围,就是3~3.5吗?
其实如果你有亲自做过实验,你就会发现一个问题,那就是你在加药前,已经就把pH值调到了3~3.5的范围。
然后再分别投加硫酸亚铁和双氧水。
但你可别忘了,硫酸亚铁是会水解的,而且其水解后是会产生H+的!
根据我的经验,10%浓度的硫酸亚铁溶液的pH值,约为3.5左右。
如果你用浓度更高的硫酸亚铁的话,那是不是水体的pH就会更低?
更别提双氧水本身也是酸性的了。
所以芬顿反应的实际pH,在经历过调酸、加亚铁和双氧水后,大多数时候其实都是低于3的。
关于这点,其实已经有很多做芬顿技术的厂家尝试了技术优化。
他们省略了最开始的原水调酸环节,只用提前调制好的硫酸亚铁溶液,就可以提供芬顿反应所需的酸环境。
再说说问题3。
问题3中,对于水中存在的,可能会与亚铁起化学反应的物质,其实可以大概分为两种情况,并分别对应着解决方法。
第一种,以防为主。
这种阴离子,主要包括硫离子、氰根离子,碳酸氢根、碳酸根、磷酸根等等。
对付它们,最好的办法就是提前做分流,让富含这些阴离子的那股水单独进行处理,去除大部分后再进芬顿系统。
第二种,就是换催化剂。
这种办法的宗旨,就是使用一些和不和上述离子沉淀的金属离子,来代替亚铁发生芬顿反应。
我们也常把其称为类芬顿技术,常见的代替催化剂就是铜。
看完了两个最主要的反应,接下来咱们再讨论下几个次要一些的副反应。
我们且来看看以下几个化学方程式。
Fe²+ + ·OH → OH- + Fe³+ (3)
RH + ·OH → R· + H2O (4)
R· + Fe³+ → R+ + Fe²+ (5)
R·+ R· → R-R (6)
R+ + O2 → ROO + →…→ CO2 + H2O (7)
先来看反应(3)。
不用我说,我估计您各位也能看出来了,这步反应其实是不利反应,却又难以避免!
只因为羟基自由基的氧化能力太强,同时亚铁的还原能力也太强,这俩根本就是干柴遇烈火,你拦也拦不住。
而反应(4)则很重要,产物也很重要,能够产生有机自由基。
而在水中,所有的自由基都是不稳定的因素,不是会引起相应的反应,就是有害于微生物。
幸好这部分的自由基是自带能量的,合理的利用会减少我们投加的药剂量,我们暂且将其看做是有利反应。
再看反应(5)。
反应(5)明显是有利反应,这种反应不浪费羟基自由基就能生成亚铁。
这也能解释前文中,我标记为蓝色字体的疑问。
也即为什么规范能够将双氧水与COD的比例定为1:1,而不是实际上的去除COD与双氧水的质量比,最高只有0.47的原因了。
正是因为有了反应(5)的存在,就相当于提高了整个芬顿的反应效率!
而水中存在的不同有机物,对应生成的有机自由基也不同,因此这部分的作用程度到底有多少,其实也不好直观评判。
有利的说完了,再说说不利的反应。
从上述反应式中,我们可以看出,R·和 R·反应可以形成较稳定的R-R,这种反应和R·还原三价铁到二价铁相比,自然就是不利反应了。
那如何才能杜绝这种不利反应呢?
有研究表明,在催化剂上构建微电场,让R·定向移动,可以有效遏制R·和 R·结合反应形成R-R。
但这个过于学术,咱们就不多言了。
其实芬顿反应的复杂程度远不止于此,至少还有很多副反应有待研究与利用。
正因如此,就连比较正规的规范,都建议让大家先实验,再确定具体的参数了。
芬顿工艺的延申领域还有很多,例如怎样提高反应效率,怎样减少产泥量,怎样减少药剂使用量等等……
这些就更让人头疼了,再此就不多赘述了。
“芬顿反应中,假设投加完亚铁时的pH值=A,反应完毕后水体的pH值=B,那么你觉得A和B,谁的值更大?
要想弄清楚这个问题的答案,你首先得明确一个原则:
“谁产生的H+越多,谁的pH就越低!”
那么芬顿反应中,会持续不断的产生氢离子,还是会持续不断的消耗氢离子呢?
接下来我揭晓下答案,一般情况下,A>B。
也即芬顿反应实际上是会持续不断产生氢离子的。
至于原因嘛,也很简单。
主要是因为三价铁和二价铁各自遇碱沉淀时,生成的Fe(OH)3,要比Fe(OH)2多消耗一个OH-。
如此一来,水中就会就是水中多出一个H+,自然水体的pH值就变低了。











精彩评论文明上网理性发言,请遵守评论服务协议
共0条评论